Создаваемый аккаунт будет индивидуальным для каждого пациента. Анкета является конфиденциальной.

Статьи
Пакет «Укус клеща»

Как только среднесуточная температура достигает +20С, начинают активизироваться клещи. Они живут в поверхностных слоях почвы, крепятся на траву и поджидают свою жертву.
Чем же опасны укусы клещей?
Как правило, клещи инфицированы микст-инфекцией. Они являются переносчиками таких тяжелых болезней, как: боррелиоз, бабезиоз, эрлихиоз, анаплазмоз, энцефалит, вирусных инфекций и др. Кроме того, множественные укусы клещей, даже не инфицированных, могут вызвать аллергические реакции.
Как определить, укусил вас клещ или другое насекомое?
Для укуса клеща характерна местная аллергическая реакции, которая выглядит на коже как округлое пятно, неправильной или правильной формы с просветлением в центре укуса.
Сам укус безболезненный для человека, поэтому длительное время может быть незамеченным.
Какие последствия могут быть после заражения инфекцией, передающейся клещом:
1. Нарушения со стороны нервной системы.
(энцефалиты, парезы, головные боли)
2. Поражения суставов (артриты, артрозы)
3. Поражения почек (гломерулонефриты, нефриты)
4. Изменения в печени (воспаления, нарушения пищеварения)
5. Заболевания легких (пневмонии и кровотечения)
Все изменения, к которым приводят укусы клещей, могут вызывать необратимые процессы, приводящие к инвалидности.
В нашей местности чаще всего встречаются клещи, инфицированные боррелиозом и анаплазмозом.
Боррелиоз – заболевание, вызываемое спирохетой боррелиоза, которые с укусом клеща попадают сначала в кожу, размножаются там и разносятся во внутренние органы (печень, почки, сердце, головной мозг, суставы и др.). Боррелии могут в течение длительного времени находиться в организме и вызывать хроническое течение заболевания. Характерным признаком является покраснение кожи в месте укуса, которое может сохраняться на протяжении 3-х недель. Через месяц начинают появляться признаки поражения нервной системы, сердца, суставов, которые могут приводить к инвалидности.
Для диагностики возможны следующие варианты анализов:
- Определение антител классов М и G. Для этого сдается кровь.
- Определение возбудителя методом ПЦР в крови, а лучше в самом клеще, если есть такая возможность.
Вовремя проведенная терапия позволяет предотвратить проявления симптомов заболевания и существенно улучшить качество жизни.
Анаплазмоз – заболевание, которое вызывается бактерией и проявляется гранулоцитарным анаплазмозом человека. Это заболевание стоит на втором месте клещевых инфекций после боррелиоза.
Бактерия с укусом клеща попадает в кровь и начинает размножаться в гранулоцитах (лейкоциты, клетки крови человека). Это сопровождается множественными циклами внедрения бактерий в клетки, в результате поражаются внутренние органы и снижается сопротивляемость организма инфекциям.
Известно, что чаще всего клещи заражены микст-инфекцией, поэтому развитие заболевания протекает более тяжело и часто с летальным исходом.
Исследование, которое поможет подтвердить или исключить наличие анаплазмы в крови или, лучше, в клеще:
- Определение возбудителя анаплазмы методом ПЦР.
Необходимо предотвращать укусы клещей, надевая защитную одежду и используя репелленты.
Сохраните свое здоровье, не медлите. Если вы подверглись укусу клеща, постарайтесь доставить клеща на исследование или сдайте кровь.
Будьте здоровы!
Авитаминоз

Авитаминоз и депрессия чреваты усиленным выпадением волос, ломкостью ногтей, сухостью кожи.
Волосы и ногти ослабли и истончились, кожа пересушена и шелушится. В коже нарушились микроциркуляция и водно-жировой баланс. Весна — это еще и время диет. Женщины стремятся привести свое тело в форму к пляжному сезону. Мы мучаем себя, изводим недоеданием. Ограничение рациона, как правило, приводит к нехватке в организме витаминов А, В5, С и Н.
Будьте с этим осторожны. Лучше проверить содержание витаминов и минералов в крови. Давайте рассмотрим значение некоторых незаменимых для организма компонентов.
· Витамин А – регулирует гормональный фон, при его недостатке наблюдается сухость кожных покровов, снижается острота зрения.
· Витамин Е (его называют «витамином молодости») – является антиоксидантом, сохраняет целостность клеточных оболочек, способствует нормализации уровня половых гормонов, снижает утомляемость.
· Витамин С – стимулирует иммунную систему, повышает эластичность кровеносных сосудов и кожи. При его недостатке наблюдается вялость, апатия.
· Витамин Д – отвечает за крепость костей, регулирует кальциевый и фосфорный обмен. При его недостатке развивается рахит. Нормализует процесс свертывания крови.
· Витамин Н – участвует в обмене веществ, необходим для роста волос, также предотвращает их выпадение и поседение. Снижает проявления сухости кожи.
· Витамин В1 – относится к нейровитаминам, регулирует все виды обмена в организме. Отвечает за остроту зрения, за восстановление кожи при стрессах, ускоряет процесс заживления ран.
· Витамин В2 – относится к нейровитаминам, участвует в сохранении блеска волос, ускоряет их рост. Предотвращает ломкость ногтей и сухость кожи.
· Витамин В3 – относится к нейровитаминам, участвует в синтезе гормонов, при достаточном уровне этого витамина кожа выглядит ухоженной, увлажненной и подтянутой.
· Витамин В6 – относится к нейровитаминам, участвует в синтезе гормонов и гемоглобина. Препятствует старению организма.
· Витамин В9 – относится к нейровитаминам, участвует в синтезе гемоглобина и многих биологически активных веществ. замедляет процессы старения кожи и выпадения волос.
· Витамин В12 – относится к нейровитаминам, отвечает за синтез гемоглобина, предупреждает старение и сухость кожи, за ломкость костей.
· Железо – участвует в тканевом и клеточном дыхании, состояние кожи напрямую зависит от количества железа в организме.
· Калий – регулирует водный баланс организма, устраняет отечность, синяки под глазами.
· Кальций – отвечает за крепость зубов, ногтей, волос. Обеспечивает нормальное функционирование клеточной оболочки, препятствует образованию морщин, участвует в нормализации pH внутренней среды.
· Магний – участвует в синтезе структурных компонентов клетки. Отвечает за давление внутри клеток и сохранение их формы, предупреждает развитие глубоких морщин.
· Марганец – поддерживает рост волос, укрепляет ногти и зубную эмаль.
· Медь – участвует в производстве коллагена, компонента кожи, который обеспечивает ее молодость и подтянутость. При недостатке этого минерала наблюдается активное выпадение волос, сухость кожных покровов.
· Селен – активатор гормонов, обеспечивает молодость коже, блестящие волосы и крепкие ногти.
· Фосфор – обеспечивает рост зубов и костей, питание кожи.
· Фтор – участвует в образовании кожи и зубной эмали. Препятствует образованию морщин.
· Хлориды – поддерживает осмотическое давление внутри клетки, препятствует ее старению, убирает отеки и темные круги под глазами.
· Хром – необходим для блеска и здоровья волос, при ломкости ногтей, восстанавливает водный и жировой баланс кожи.
· Цинк – способствует здоровой коже, крепким ногтям и волосам. При его недостатке появляются белые полосы на ногтях.
Известно, что каждый из вышеперечисленных минералов жизненно необходим для нормальной жизнедеятельности организма, его эффективного функционирования. Если какого-либо элемента не хватает, это может тяжело сказаться на здоровье человека. Если уровень микроэлементов недостаточный, с большой вероятностью могут возникнуть следующие проблемы: ослабевание защитных сил организма, разнообразные заболевания кожи, сахарный диабет, заболевания волос, зубов, ногтевых пластин, ожирение, костные недуги (сколиоз, остеопороз), анемия. Могут возникнуть проблемы с сердцем и сосудами, с репродукцией, потенцией, половым влечением. Приостанавливается развитие.Нехватка микроэлементов может возникнуть в случае, если Вы:
· употребляете питьевую воду низкого качества, несбалансированно питаетесь;
· проживаете в районе с неблагополучной экологией;
· перенесли кровотечение и, как результат – огромную потерю минералов;
· принимали лекарства, которые разрушили микроэлементы.
Мы рекомендуем не заниматься самолечением. Если Вы имеете проблемы с кожей, ногтями, волосами или чувствуете постоянную усталость, посетите врача и проверьте уровень витаминов и минералов в организме.
Гликозилированный гемоглобин
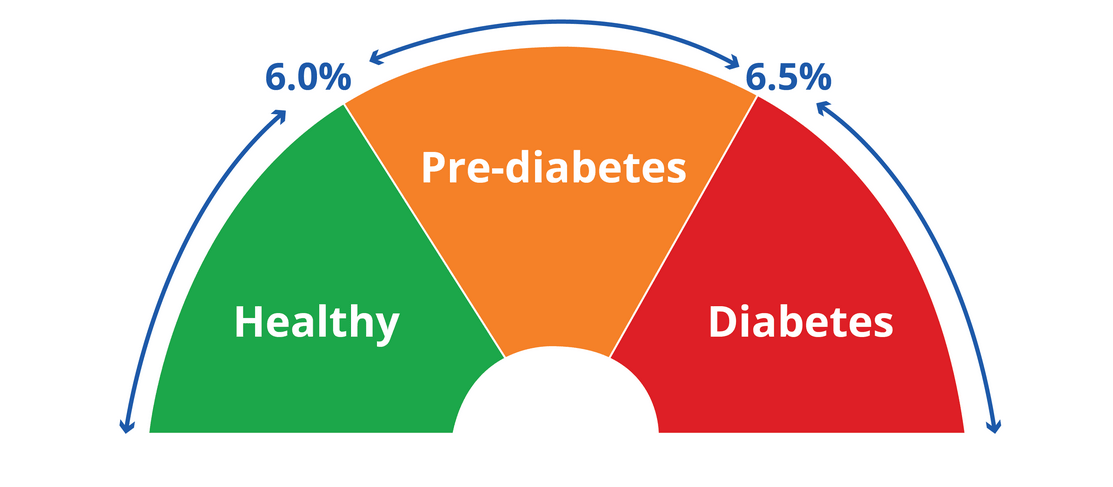
(HbA1C, GlycatedHemoglobin)
Соединение гемоглобина с глюкозой, позволяющее оценивать уровень гликемии за 1-3 месяца, предшествующие исследованию.
Образуется в результате медленного неферментативного присоединения глюкозы к гемоглобину А, содержащемуся в эритроцитах
Эритроциты, циркулирующие в крови, имеют разный возраст. Обычно ориентируются на усредненный срок - 60 суток. Уровень гликозилированного гемоглобина является показателем компенсации углеводного обмена на протяжении этого периода. Нормализация уровня гликозилированного гемоглобина в крови происходит на 4-6-й неделе после достижения нормального уровня глюкозы.
В соответствии с рекомендациями ВОЗ этот тест признан оптимальным для контроля сахарного диабета. Таким больным рекомендуется проводить исследование уровня гликозилированного гемоглобина не менее одного раза в квартал.
Результаты теста могут быть ложно изменены при любых состояниях, влияющих на средний срок жизни эритроцитов крови. Кровотечения или гемолиз вызывают ложное снижение результата; гемотрансфузии, естественно, искажают результат; при железодефицитной анемии наблюдается ложное повышение результата определения гликозилированного гемоглобина.
Показания к назначению анализа
Долговременный мониторинг течения и контроля при лечении больных сахарным диабетом, а также для определения степени компенсации заболевания.
Подготовка к исследованию
Взятие крови желательно производить натощак. Исследование нецелесообразно проводить после кровотечений, гемотрансфузии.
Повышение значений
- Сахарный диабет и другие состояния, которые сопровождаются нарушением толерантности к глюкозе.
- Дефицит железа.
- Спленэктомия. Ложное повышение может быть обусловлено высокой концентрацией фетального гемоглобина (HbF).
Снижение значений
- Гипогликемия.
- Гемолитическая анемия.
- Кровотечения.
- Переливание крови.
Рак яичников. Ранняя диагностика
Использование маркеров СА125 и HE4 в диагностике
Риск развития рака яичников повышается с возрастом и снижается во время беременности. Риск выявления этого заболевания в течение жизни составляет1.6%, в случае неблагоприятной наследственности (наличие рака яичников у лиц первой степени родства) этот показатель возрастет до 5%, у носительниц мутации гена BRCA1 или BRCA2 или имевших в анамнезе неполипозный рак кишечника (синдром Линча, Lynch syndrome) – до 25-60% в зависимости от характера выявленной мутации. Однако следует помнить, что рак яичников – «тихий убийца» - особенно часто поражает женщин старше 50 лет, не имеющих жалоб, хотя нечеткие неспецифические симптомы нередко присутствуют. При проведении обследования нельзя забывать, что у женщин с неблагоприятной наследственностью по раку яичника, кроме того, повышается риск рака молочных желез и кишечника.
В качестве новых диагностических маркеров предложен также HE4 (человеческий эпидидермальный протеин 4, Human epididymis protein 4 – протеаза, уровень которой возрастает у женщин с эпителиальным раком, по чувствительностипочти не уступающая СА 125.
Уровни СА125, НЕ4 начинают незначительно повышаться за три года до постановки диагноза, однако значимое повышение отмечается только за год до диагностирования образования.
Уровень CA125 в сыворотке крови считается единственным надежным маркером для рака яичников, полезным в ходе динамического наблюдения за пациентками, оценки эффективности терапии и рецидивов. Тем не менее, его нельзя отнести к идеальным диагностическим и прогностическим маркерам. Определение уровня CA125 в качестве единственного методадиагностики обладает низкой чувствительностью ,поскольку повышение уровня CA125 может отмечаться при следующих гинекологических ситуациях: первый триместр беременности, воспалительные заболевания органов малого таза : миома матки, кисты яичников, спаечный процесс в малом тазу и эндометриоз.
Так как эти ситуации не характерны для женщин в постменопаузе, измерение уровня CA125 в этой популяции приобретает большее значение по сравнению с молодыми женщинами. Кроме того, несколько измерений уровня этого
маркера с перерывом в 3-4 недели и повышение его значений может характеризовать прогрессирование процесса малигнизации, в то время как при доброкачественных образованиях его уровень остается стабильным
или снижается. В любом случае следует помнить, что этот показатель может меняться по-разному в зависимости от типа опухоли и даже при низких его значениях может диагностироваться рак яичников.
Роль HE4 (человеческий эпидидемальный протеин 4)
Рак яичников является наиболее распространенной формой рака у женщин репродуктивного возраста во всем мире, а также основной причиной смертности от гинекологических злокачественных опухолей. При обнаружении заболевания на ранних стадиях прогноз благоприятный. Однако в 70%
случаев заболевание диагностируется на более поздних стадиях, когда выживаемость очень низка. Только 10-30% таких пациентов живут более года. В настоящее время диагностические операции, проводящиеся квалифицированным онкогинекологом, доступны менее чем половине больных раком яичников, что еще больше снижает выживаемость. Для направления пациента к соответствующему специалисту может быть использован
комплексный тест, сочетающий анализ на СА125 и HE4. HE4 (человеческий эпидидермальный протеин 4) является ценным биомаркером для выявления рака яичников и характеризуется минимальной экспрессией в нормальной
ткани яичников. В дополнение к экспрессии на клеточном уровне высокие уровни секреции HE4 были обнаружены в сыворотке больных раком яичников.
При сравнении здоровых людей и больных раком яичников специфичность HE4 достигает 96%, а чувствительность 80%. Таким образом, комбинация определений HE4 и CA125 является более точным предиктором присутствия злокачественного образования, чем любой из маркеров
в отдельности или комбинация любых других маркеров. Результаты должны интерпретироваться в совокупности с результатами других исследований в соответствии со стандартными клиническими руководствами.
Кроме того, НЕ4 может быть использован для мониторинга эффективности терапии при инвазивном эпителиальном раке яичников. Результаты должны быть использованы в сочетании с другими клиническими методами, используемыми
для мониторинга рака яичников.
Ограничения метода
У пациенток с подтвержденным диагнозом рак яичника значения НЕ4 могут находиться в одном диапазоне со значениями, определяемыми у здоровых женщин. Отдельные гистологические типы рака яичника, такие как герминогенные и мукоидные, редко экспрессируют НЕ4, следовательно, НЕ4 не может быть рекомендован для мониторинга пациенток с диагностированными герминогенными или мукоидными опухолями яичников. Кроме того, повышенные уровние антигена НЕ4 могут присутствовать у женщин, не страдающих злокачественными заболеваниями. Следовательно, уровень НЕ4 не может быть использован как абсолютное доказательство отсутствия или присутствия злокачественного образования и изолированное определение НЕ4 не должно быть использовано для скрининга рака. При постановке диагноза и мониторинге заболевания результаты тестирования должны интерпретироваться в совокупности с результатами других исследований и диагностических процедур, тест НЕ4 не должен заменять какую-либо установленную клиническую процедуру.
Алгоритм расчета риска злокачественной опухоли яичников не был доказан для следующих групп пациенток:
- женщины, уже проходившие курс лечения по поводу злокачественной опухоли,
- женщины, проходящие курс химиотерапии,
- пациентки моложе 18 лет.
Алгоритм математического расчета риска злокачественной опухоли яичника (Risk of Ovarian Malignancy Algorithm, ROMA) для оценки риска эпителиального рака яичника у женщин в пре- ипостменопаузе, при выявлении образований в малом тазу.
Интерпретация результатов ROMA (Risk Ovarian Malignancy
Algorithm) с использованием тестов НЕ4 и CA125
Разделение на группы высокого и низкого риска
Женщины в пременопаузе:
ROMA > 12,9% - высокий риск обнаружения эпителиального РЯ
ROMA < 12,9% - низкий риск обнаружения эпителиального РЯ
Женщины в постменопаузе:
ROMA > 24,7% - высокий риск обнаружения эпителиального РЯ
ROMA < 24,7% - низкий риск обнаружения эпителиального РЯ
Расчет ROMA предоставляется вместе с результатами тестов СА125 и НЕ4 в лабораторном отчете.
Панель контроля анемии
Витамин В12 (цианокобаламин, кобаламин, СоЬаlатiт)
Витамин, необходимый для нормального кроветворения (образования и созревания эритроцитов)
Витамин В12 в организме человека не синтезируется. Источниками являются кишечная микрофлора, а также продукты животного происхождения (дрожжи, молоко, мясо, печень, почки, рыба и яичный желток). Женское молоко содержит витамин В12 в виде метилкобаламина - основной формы, в которой витамин находится в организме человека. Во время переваривания в желудке цианокобаламин связывается с внутренним фактором Каста -белком, который синтезируется париетальными клетками слизистой оболочки желудка, вырабатывающими также и соляную кислоту. В восходящем отделе подвздошной кишки этот комплекс всасывается; в клетках слизистой витамин В12 высвобождается и связывается с белком -транскобаламином, который доставляет цианокобаламин в печень и другие ткани. Основным местом депонирования витамина В12 является печень. Большое количество его поглощается селезенкой и почками, несколько меньше - мышцами. Общие запасы кобаламина в организме взрослого человека составляют около 2-5 мг. Метаболизм витамина происходит очень медленно. Выводится он желчью, в кишечнике основная часть его реабсорбируется, т.е. ему свойственна энтерогепатическая циркуляция. Для развития дефицита витамина при сниженном поступлении его в организм требуется длительное время: около 5-6 лет.
Витамин В12 играет важную роль в процессах метаболизма, в составе кобаламиновых ферментов участвует в белковом, жировом и углеводном обмене. Витамин В12 имеет две коферментные формы: метилкобаламин и дезоксиаденозилкобаламин (кобамамид). Основная функция активных форм коферментов - перенос метильных одноуглеродных групп (трансметилирование). Участвуют в обмене белков и нуклеиновых кислот (синтез метионина, ацетата, дезокси-рибонуклеотидов). Цианокобаламин является коэнзимом, который играет важную роль в метаболизме фолиевой кислоты, в частности, участвует в ее транспорте в клетки. При участии метилкобаламина в организме синтезируется активная форма фолиевой кислоты, которая принимает участие в образовании пиримидиновых и пури-новых оснований, нуклеиновых кислот. При недостатке кобаламина наиболее выраженные изменения развиваются в пролиферирующих клетках, например, в клетках костного мозга, полости рта, языка и желудочно-кишечного тракта, что ведет к нарушению кроветворения, глоссита, стоматита и кишечной мальабсорбции. Витамин В12 также способствует накоплению в эритроцитах сульфгид-рильных групп, главным образом глутатиона, поэтому его недостаток ведет к нарушению деления и созревания эритроцитов и развитию мегалобластической анемии. Витамин В12 является кофактором фермента гомоцистеинметилтрансферазы, участвующей в превращении гомоцистеина в метионин. Метионин важен для синтеза фосфолипи-дов и миелиновой оболочки нейронов, поэтому дефицит витамина В12 сопровождается неврологической симптоматикой (психические расстройства, полиневриты, фуникулярный миелоз - поражение спинного мозга). Неврологические симптомы дефицита витамина В12 различны в зависимости от тяжести патологии. К ранним признакам относится дисфункция задних рогов спинного мозга с нарушением походки. Позже у них развивается поражение пирамидного, спиномозжечкового и спиноталамического трактов, сопровождающееся мышечной слабостью, прогрессирующей спастичностью, гиперрефлексией, «ножницеобразной» походкой. При длительном дефиците витамина В12 возникают деменция и нейропсихические заболевания. Цианокобаламин принмает участие в синтезе холина и метионина, оказывает благоприятное воздействие на печень, предупреждает развитие жирового гепатоза.
Аденозилкобаламин служит коэнзимом метилмалонил-КоА-мутазы -фермента для превращения метилмалоновой кислоты в сукцинило-вую кислоту. Значительное ингибирование этой реакции ведет к развитию опасного для жизни состояния - метилмалоновой ацидурии. Клинически это состояние проявляется значительным отставанием ребенка в весе, сниженной толерантностью к белкам, кетоацидозом, гипогликемией, гипераммониемией и гиперглицинемией, высоким содержанием метилмалоновой кислоты в моче. Заболевание не сопровождается развитием межобластной анемии. Нарушения метаболизма витамина В12 наблюдаются у младенцев, страдающих генетически обусловленным дефектом ферментов, необходимых для превращения витамина В12 в кофермент, или низким уровнем плазменного белка-переносчика. Развивающаяся при этом межобластная анемия проявляется уже в первые недели или месяцы жизни и характеризуется нормальным или чуть сниженным уровнем витамина В12 в крови. В отличие от нее при анемии, развивающейся в результате нарушений всасывания, всегда выявляется низкий уровень витамина В12. Дефицит цианокобаламина часто развивается у пожилых людей, проявляется неврологическими нарушениями.
Показания к назначению анализа
Дифференциальная диагностика макроцитарных анемий;
Хронические воспалительные заболевания и анатомические пороки тонкой кишки, атрофический гастрит;
Диагностика врожденных форм дефицита витамина В12;
Контроль состояния при строгой вегетарианской диете;
Подготовка к исследованию: Взятие крови производится натощак.
Повышение уровня витамина В12
Заболевания печени (острый и хронический гепатит, цирроз печени, печеночная кома, при которой уровень может превышать норму в 30-40 раз);
Эритролейкемия;
Метастазы злокачественных опухолей в печень;
Повышенный уровень транскобаламина (несмотря на возможное истощение запасов витамина в печени);
Хроническая почечная недостаточность;
Острый и хронический миелолейкоз, моноцитарный лейкоз.
Понижение уровня витамина В12 Недостаточное поступление витамина В12 в организм:
Строгая вегетарианская диета;
Низкое содержание витамина в женском молоке (причина мегалобластической анемии у младенцев);
Алкоголизм;
Нарушение всасывания кобаламинов:
Синдром мальабсорбции (целиакия, спру);
Резекция различных участков ЖКТ (желудка, тонкой кишки);
Хронические воспалительные заболевания и анатомические пороки тонкой кишки, атрофический гастрит;
Паразитарные инвазии (особенно, вызванная широким лентецом - дифиллоботриоз);
Болезнь Аддисона - Бирмера (пернициозная анемия -недостаточность внутреннего фактора Кастла);
Болезнь Альцгеймера;
Врожденные нарушения метаболизма кобаламинов:
Оротовая и метилмалоновая ацидурия;
Дефицит транскобаламина;
Синдром Иммерслунда - Гресбека (врожденное нарушение транспорта витамина В12 через кишечную стенку, сопровождается протеинурией).
Дефицит фолиевой кислоты
Прием лекарственных препаратов (например, аминогликози-дов, неомицина, противосудорожных средств (фенобарбитал), холестирамина, оральных контрацептивов, ранитидина).
Ферритин(Ferritin)
Самый информативный индикатор запасов железа в организме, основная форма депонированного железа.
Представляет собой белок - апоферритин. Одна молекула ферритина может содержать до 4000 молекул железа. Фер-ритин синтезируется в клетках органов ретикуло-эндотелиаль-ной системы. Ферритин сыворотки содержит 20-25% железа; его концентрация - показатель запасов железа у здоровых людей и при неосложненных железодефицитных состояниях. Во время беременности уровень ферритина может снижаться постепенно, на 50% к 20-й неделе, на 70% в третьем триместре беременности. В условиях острого воспаления повышенный уровень сывороточного ферритина может быть проявлением острофазного ответа, так как ферритин является одним из острофазных белков. Тем не менее, если у пациента действительно имеется дефицит железа, острофазное повышение трансферрина не бывает значительным.
Определение концентрации ферритина так же важно для дифференциальной диагностики железодефицитной анемии и анемии хронических заболеваний. Одним из основных механизмов таких анемий является перераспределение железа в клетки макрофагальной системы. Железо накапливается в макрофагах в виде ферритина, перенос его от ферритина к трансферрину нарушается, что влечет за собой снижение уровня сывороточного железа. В этих условиях ошибочный диагноз железодефицитной анемии и назначение препаратов железа может привести к развитию вторичного гемосидероза и усугублению положения больного. Дифференциальная диагностика истинного и перераспределительного дефицита железа возможна только при условии определения уровня сывороточного ферритина. При онкопатологии, особенно опухолевых и метастатических поражениях костного мозга, ферритин служит своеобразным опухолевым маркером. К временному значительному повышению уровня сывороточного ферритина приводит избыточное поступление железа после трансфузий или гемодиализа.
Показания к назначению анализа:
Подозрение на гемохроматоз.
Дифференциальная диагностика анемии;
Опухоли
Хронические инфекционные и воспалительные заболевания.
Подготовка к исследованию: Натощак.
Повышение уровня ферритина:
Избыток железа при гемохроматозе;
Патология печени (в т.ч. алкогольный гепатит);
Острый лимфобластный и миелобластный лейкоз;
Острые и хронические инфекционно-воспалительные заболевания (остеомиелит, легочные инфекции, ожоги, системная красная волчанка, ревматоидный артрит);
Лимфогранулематоз;
Рак молочной железы;
Голодание;
Прием оральных контрацептивов
Понижение уровня ферритина:
Дефицит железа (железодефицитная анемия);
Целиакия.
Фолиевая кислота (FolicAcid)
Витамин, необходимый для нормального гемопоэза (кроветворения).
Источник - микрофлора кишечника, частично поступает с пищей (шпинат, салат-латук, бобы, спаржа, зерновые, мука грубого помола). Является кофактором ферментов, участвующих в синтезе пуриновых и пиримидиновых оснований, ДНК и РНК, в синтезе белков, аминокислот (метионина, серина), в обмене холина. Фолиевая кислота играет важное значение в процессах митоза; способствует соединению белковой группы и гема в гемоглобине и миоглобине. Стимулирует эритро-, лейко- и тромбоцитопоэз, пластические и регенераторные процессы во всех органах и тканях. Уровень концентрации фолиевой кислоты в сыворотке отражает ее поступление с пищей. Оказывает также антиатеросклеротическое, онкопротекторное и ноотропное действие.
Недостаток фолиевой кислоты тормозит переход мегалобластической фазы кроветворения в нормобластическую и приводит к мегалобластической анемии (увеличение объема эритроцитов). У детей с дефицитом фолиевой кислоты наблюдается отставание в весе, угнетается функция костного мозга, нарушается нормальное созревание слизистой оболочки желудочно-кишечного тракта, кожных покровов, что создает основу для развития энтеритов, опрелостей, задержки психомоторного развития.
Дефицит фолиевой кислоты у беременных является пусковым фактором для развития невынашивания, частичной или полной отслойки плаценты, спонтанного аборта или мертворождения, повышает риск развития у плода врожденных пороков, в частности дефектов нервной трубки, гидроцефалии, анэнцефалии, мозговых грыж и т.п.; увеличивает риск задержки умственного развития ребенка. Запасы фолиевой кислоты в печени относительно невелики, в связи с чем ее дефицит может развиться в течение 1 мес после прекращения ее поступления, а анемия - через 4 мес.
Показания к назначению анализа:
Диагностика и дифференциальная диагностика макроцитарных анемий;
Диагностика нарушений со стороны крови (анемии и лейкопении), вызванных химиотерапией или лучевой терапией.
Подготовка к исследованию: забор крови производится натощак.
Повышение уровня фолиевой кислоты :
Вегетарианская диета;
Пернициозная анемия (дефицит витамина В12);
Заболевания дистального отдела тонкой кишки;
Синдром приводящей петли.
Понижение уровня фолиевой кислоты:
Недостаточное поступление с пищей или нарушение всасывания:
Недостаток фолиевой кислоты в рационе питания;
Анорексия;
Алкоголизм;
Нарушение всасывания при синдроме мальабсорбции, целиакии, спру, энтерите, резекции желудка и кишечника;
Прием препаратов, нарушающих всасывание фолиевой кислоты (аспирина, противосудорожных препаратов, эстрогенов, нитрофуранов, пероральных контрацептивов, антацидов, холестирамина, сульфасалазина) и ее антагонистов (триметоприма, метотрексата, азатиоприна, азидотимидина).
Повышенное потребление или потеря при нормальном поступлении с пищей:
Беременность, лактация;
Периоды интенсивного роста;
Пожилой возраст;
Лихорадка, септические состояния;
Гемолитические анемии;
Злокачественные опухоли;
Гипертиреоз у детей;
Миелопролиферативные заболевания;
Сидеробластическая анемия;
Заболевания печени;
11.Гемодиализ.
Железо (Fe, Iron)
Микроэлемент, участвующий в процессе связывания, переноса и передачи кислорода в ткани и в процессах тканевого дыхания.
Железо входит в состав дыхательных пигментов (преимущественно - гемоглобина, и частично - миоглобина), цитохромов, железосодержащих ферментов (каталазы, миелопероксидазы). Это так называемое, гемовое железо, которое обратимо связывает кислород и участвует в транспорте кислорода, ряде окислительно-восстановительных реакций, играет важную роль в процессах кроветворения. Железо принимает участие в метаболизме порфирина, синтезе коллагена, поддержании иммунного статуса. В организм железо поступает с пищей. В пищевых продуктах железо присутствует или в виде составной части гема (мясо, рыба) или как негемовое железо (овощи, фрукты). Из пищи усваивается около 10-15 % железа, всасывание происходит в 12-перстной кишке. Общее содержание железа в организме -4-5 г. Около 70% железа входит в состав гемоглобина, 5% -миоглобина, 20% находится в депо (печени, селезенке, костном мозге) в виде растворимого ферритина и нерастворимого гемосидерина. Всасывание железа регулируется энтероцитами: оно возрастает при дефиците железа, неэффективном эритропоэзе и блокируется при избытке железа в организме. Транспорт железа от кишечной стенки до предшественников эритроцитов и клеток-депо (макрофагов) осуществляется плазменным белком - трансферрином. В организме железо не встречается в виде свободных катионов, только в связанном виде с белками.
Концентрация железа в сыворотке зависит от резорбции в желудочно-кишечном тракте, накоплений в кишечнике, селезенке и костном мозге, от синтеза и распада гемоглобина и его потери организмом. Уровень железа в сыворотке изменяется в течение суток (наиболее высок он утром), зависит от пола и возраста. У новорожденных в течение нескольких часов после родов отмечается падение уровня железа. Средние показатели железа у женщин ниже, чем у мужчин, но и у тех и у других с возрастом показатель железа падает. Концентрация железа у женщин также связана с менструальным циклом (максимальное содержание - в лютеиновую фазу, самое низкое - после менструации). Недостаток сна и стрессы, выраженная физическая нагрузка также вызывают снижение этого показателя. При беременности содержание железа в организме уменьшается, особенно во II и III триместре беременности (повышение потребности в железе в этот период связано с формированием депо железа у плода).
Несмотря на нестабильность уровня железа в сыворотке, исследование этого параметра важно для скрининга, дифференциальной диагностики железодефицитных и других анемий, а также оценки эффективности лечения больных железодефицитными анемиями. Выраженный дефицит железа сопровождается снижением уровня гемоглобина и цветного показателя. Выраженное снижение концентрации железа в сыворотке крови может быть отмечено при дефиците железа в организме, но для диагностики латентной анемии недостаточно определения содержания железа в сыворотке крови. Для более точной оценки баланса железа в организме необходимо провести дополнительные исследования (ферритин, трансферрин и пр.).
Показания к назначению анализа:
Диагностика и дифференциальная диагностика анемий различной этиологии, контроль терапии железодефицитной анемии;
Острые и хронические инфекционные заболевания, системные воспалительные заболевания;
Нарушение питания и всасывания, гипо- и авитаминозы, нарушения со стороны желудочно-кишечного тракта;
Возможное отравление железосодержащими препаратами.
Подготовка к исследованию: Натощак. Для получения корректных результатов необходимо прекратить прием железосодержащих лекарственных препаратов. Если пациенту было проведено переливание крови, исследование необходимо отложить на несколько дней.
Повышение уровня железа: Повышенное поступление в организм:
Гемохроматоз;
Избыточное парентеральное введение препаратов железа;
Повторные гемотрансфузии;
Острое отравление препаратами железа;
Анемии:
Гемолитические анемии,
Гипо- и апластические анемии;
Витамин В12 (и В6) - и фолиево-дефицитные гиперхром-ные анемии;
Талассемия;
Нефрит;
Заболевания печени (острый гепатит, хронический гепатит) - вследствие недостаточного использования железа в синтезе гема;
Острая лейкемия;
Свинцовая интоксикация;
Применение таких лекарственных средств, как левомицетин, эстрогены, оральные контрацептивы, метотрексат, цисплатин.
Понижение уровня железа:
Железодефицитная анемия;
Острые и хронические инфекционные заболевания, сепсис, коллагенозы;
Опухоли (в т.ч. острый и хронический лейкозы, миелома);
Повышенные потери железа организмом (острые и хронические кровопотери);
Недостаточное поступление железа в организм (молочно-растительная диета, синдром мальабсорбции, заболевания желудка и кишечника);
Повышенное потребление железа организмом (беременность, кормление грудью, подростковый период, повышенные физические нагрузки);
Ремиссия пернициозной анемии (авитаминоз В12);
Гипотиреоз;
Нефротический синдром;
Хронические заболевания печени (гепатит, цирроз);
Прием аллопуринола, андрогенов, аспирина, холестирамина, глюкокортикоидов.
Общая железосвязывающая способность сыворотки(ОЖСС).
ОЖСС-лабораторный тест, который дает возможность определить степень насыщения железом сыворотки.
Повышение уровня ОЖСС:
-гипохромные анемии, острый гепатит. Поздние сроки беремрнности;
-прийом эстрогенов, пероральных контрацептивов.
Понижение уровня:
-анемия(не железодефицитная), хронические инфекции, гемохроматоз, цирроз, неопластические и почечные заболевания,талласемия,
-прийом аспарагиназы,хлорамфеникола, кортикотропина, кортизрона.